Меню змесціва
● Уводзіны ў карбід вальфрама
>> Хімічная структура
● Сінтэз карбіду вальфраму
● Хімічныя ўласцівасці і рэактыўнасць
● Прымяненне карбіду вальфрама
● Пашыраны прыкладанні
● Праблемы і будучыя напрамкі
● Уплыў на навакольнае асяроддзе
● Выснова
● FAQ
>> 1. Што такое карбід вальфраму?
>> 2. Як сінтэзуецца карбід вальфрама?
>> 3. Ці рэагуе на кіслоты карбіду вальфрама?
>> 4. Якія асноўныя прыкладанні карбіду вальфраму?
>> 5. Ці можна перапрацаваць карбід вальфраму?
● Цытаты:
Карбід вальфраму - гэта злучэнне, вырабленае з вальфрама і вугляроду, які славіцца выключнай цвёрдасцю, зносам і даўгавечнасці. Ён шырока выкарыстоўваецца ў прамысловых дадатках, уключаючы рэжучыя інструменты, буравыя біты і ўстойлівыя да зносу кампанентаў. Аднак разуменне яго рэактыўнасці мае вырашальнае значэнне для яго бяспечнага і эфектыўнага выкарыстання. У гэтым артыкуле мы паглыбімся ў рэактыўнасць Карбід вальфраму , вывучаючы яго хімічныя ўласцівасці, метады сінтэзу і прымяненне.

Уводзіны ў карбід вальфрама
Карбід вальфраму-гэта шчыльнае, металічнае рэчыва са светла-шэрым колерам і сіняватым адценнем. Ён рыхтуецца пры награвальным вальфраме з вугляродным чорным пры наяўнасці вадароду пры высокіх тэмпературах (ад 1400 ° С да 1600 ° С). Атрыманае злучэнне надзвычай цвёрды, рэйтынг каля 9,0 да 9,5 па шкале MOHS, што робіць яго адным з самых складаных матэрыялаў.
Хімічная структура
Карбід вальфраму ўтварае шасцігранную крыштальную структуру, якая спрыяе яго цвёрдасці і ўстойлівасці. Злучэнне ў асноўным складаецца з вальфрама і вугляроду ў суадносінах 1: 1, часта змешаным з металічным злучным, як кобальт, каб павысіць яго трываласць і даўгавечнасць.
Сінтэз карбіду вальфраму
Сінтэз карбіду вальфраму ўключае ў сябе некалькі метадаў:
1. Рэакцыя высокай тэмпературы: метал вальфраму або парашок рэагуе з вугляродам пры тэмпературы паміж 1400 ° С і 2000 ° С.
2. Працэс вадкасці: Гэты метад выкарыстоўвае больш нізкую тэмпературу (900 ° С да 1200 ° С) і ўключае ў сябе ўзаемадзеянне вальфрамавага металу або сіняга аксіду вальфрама (WO 3) з газавай сумессю CO/CO 2 і вадародам.
3. Хімічнае адкладанне пары (ССЗ): гексахларыд вальфраму рэагуе з вадародам і метанам пры 670 ° С, утвараючы карбід вальфраму.
WCL6 + 6H 2 + CH 4 → WC + 6HC
Хімічныя ўласцівасці і рэактыўнасць
Карбід вальфраму вельмі ўстойлівы і ўстойлівы да карозіі пры звычайных тэмпературах. Аднак у пэўных умовах ён рэагуе з пэўнымі рэчывамі:
- Акісленне: карбід вальфраму пачынае акісляцца пры тэмпературы ад 500 ° С да 600 ° С, утвараючы трыаксід вальфраму (WO3) пры награванні ў атмасферы, якая змяшчае кісларод.
- Кіслотная ўстойлівасць: яна ўстойлівая да большасці кіслот, але раствараецца ў сумесі азотнай кіслаты і гідрафторнай кіслаты.
Wc + hno 3/hf → раствараецца
- Галогенавыя рэакцыі: карбід вальфраму ўступае ў рэакцыю з фторам пры пакаёвай тэмпературы і з хлорам вышэй 400 ° С.
Прымяненне карбіду вальфрама
Дзякуючы выключнай цвёрдасці і зносу, карбід вальфраму выкарыстоўваецца ў розных дадатках:
1. Рэжучыя інструменты і буравыя біты: яго здольнасць падтрымліваць рэзкасць ва ўмовах высокага стрэсу робіць яго ідэальным для рэзкі інструментаў і свідравання біт.
2. Ювелірныя вырабы: Карбід вальфраму таксама выкарыстоўваецца ў ювелірных вырабах з -за яго трываласці і эстэтычнай прывабнасці.
3
4. Аўтамабільная і аэракасмічная: карбід вальфраму выкарыстоўваецца ў гэтых сектарах для сваёй высокай трываласці і супраціву да зносу, што спрыяе даўгавечнасці кампанентаў.
5. Медыцынскія інструменты: Ён выкарыстоўваецца ў хірургічных інструментах для яго цвёрдасці і ўстойлівасці да карозіі.
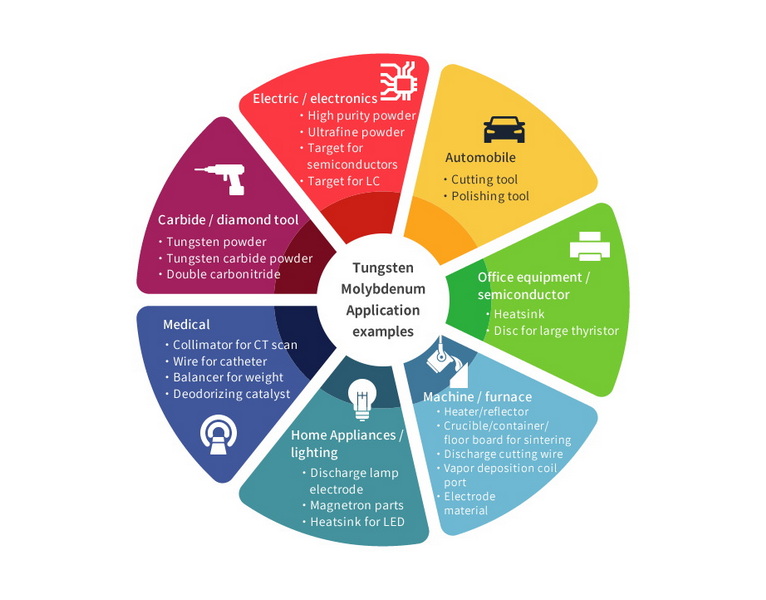
Пашыраны прыкладанні
У апошнія гады карбід вальфраму заўважыў поспехі ў сваіх дадатках:
-Каталіз: Карбід вальфраму вывучаецца як каталізатар рэакцый гідрагенацыі з-за яго плацінападобных уласцівасцей, прапаноўваючы эканамічную альтэрнатыву мадэрнізацыі біямасы [7].
- Захоўванне энергіі: Даследаванне матэрыялаў на аснове вальфрамавага карбіду для прылад захоўвання энергіі працягваецца, выкарыстоўваючы высокую праводнасць і стабільнасць.
Праблемы і будучыя напрамкі
Нягледзячы на свае шматлікія перавагі, карбід вальфраму сутыкаецца з такімі праблемамі, як далікатнасць і неабходнасць злучнага ўзмацнення трываласці. Будучыя даследаванні накіраваны на паляпшэнне ўмоў сінтэзу і вывучэнне новых прыкладанняў у новых галінах, такіх як аднаўляльныя крыніцы энергіі і перадавыя матэрыялы.
Уплыў на навакольнае асяроддзе
Перапрацоўка карбіду вальфраму мае вырашальнае значэнне для зніжэння адходаў і захавання рэсурсаў. Для мінімізацыі ўздзеяння на навакольнае асяроддзе распрацоўваюцца метады аднаўлення і паўторнага выкарыстання зношаных інструментаў.
Выснова
Карбід вальфраму - гэта вельмі ўстойлівае злучэнне з выключнай цвёрдасцю і зносам. Хоць ён звычайна не рэактыўны пры нармальных тэмпературах, ён можа рэагаваць з пэўнымі рэчывамі пры пэўных умовах. Разуменне яго хімічных уласцівасцей і рэактыўнасці мае вырашальнае значэнне для яго эфектыўнага выкарыстання ў розных прамысловых і спажывецкіх прыкладаннях.

FAQ
1. Што такое карбід вальфраму?
Карбід вальфраму - гэта злучэнне, вырабленае з вальфрама і вугляроду, вядомы сваёй цвёрдасцю і зносам. Ён выкарыстоўваецца ў рэжучых інструментах, буравых бітах і іншых устойлівых да зносу кампанентаў.
2. Як сінтэзуецца карбід вальфрама?
Карбід вальфраму сінтэзуецца, рэагуючы вальфраму з вугляродам пры высокіх тэмпературах альбо метадамі адкладу хімічных пары.
3. Ці рэагуе на кіслоты карбіду вальфрама?
Карбід вальфраму ўстойлівы да большасці кіслот, але раствараецца ў сумесі азотнай кіслаты і гідрафторнай кіслаты.
4. Якія асноўныя прыкладанні карбіду вальфраму?
Карбід вальфраму ў асноўным выкарыстоўваецца ў рэжучых інструментах, буравых бітах, кампанентах прамысловай тэхнікі, ювелірных вырабаў і медыцынскіх інструментаў з -за яго цвёрдасці і даўгавечнасці.
5. Ці можна перапрацаваць карбід вальфраму?
Так, карбід вальфраму можна перапрацаваць. Знесеныя інструменты і металалом могуць быць адноўлены і паўторна выкарыстаны, зніжаючы адходы і захаванне рэсурсаў.
Цытаты:
[1] https://www.science.gov/topicpages/t/tungsten+carbide+leaching.html
[2] https://www.refractorymetal.org/tungsten-carbide-uses-properties.html
[3] https://www.linkedin.com/pulse/applications-tungsten-carbide-zzbettercarbide
[4] https://www.alamy.com/stock-photo/tungsten-carbide.html
[5] https://en.wikipedia.org/wiki/tungsten_carbide
[6] https://create.vista.com/photos/tungsten-carbide/
[7] https://www.ch.nat.tum.de/en/ac4/research-topics/tungsten-carbide/
Ці
[9] https://www.gettyimages.hk/%E5%9C%96%E7%89%87/tungsten-carbide?page=2
[10] https://www.chemicalbook.com/chemicalproductproperty_en_cb5174366.htm
[11] https://chemistry-europe.onlinelibrary.wiley.com/doi/10.1002/celc.202300722
[12] https://www.allied-material.co.jp/en/techinfo/tungsten_carbide/features.html
[13] https://www.mdpi.com/1420-3049/30/1/84
[14] https://www.sollex.se/en/blog/post/tungsten-carbide-and-technology-part-2
[15] https://pubs.acs.org/doi/10.1021/acsomega.8b03449
[16] https://www.azom.com/article.aspx?articleid=1203
[17] https://www.nature.com/articles/S41467-018-03429-Z
[18] https://www.carbideprobes.com/wp-content/uploads/2019/07/tungstencarbidedatasheet.pdf
[19] https://www.samaterys.com/content/application-of-tungsten-in-modern-industry.html
[20] https://www.imetra.com/tungsten-carbide-material-properties/
[21] https://www.azom.com/properties.aspx?articleid=1203
[22] https://www.freepik.com/free-photos-vectors/tungsten
[23] https://www.istockphoto.com/photos/tungsten-carbide
[24] https://stock.adobe.com/search?k=tungsten+carbide
[25] https://www.gettyimages.hk/%E5%9C%96%E7%89%87/tungsten-carbide
[26] https://www.shutterstock.com/search/tungsten
[27] https://cen.acs.org/materies/chemistry-pictures-tungsten-carbide-slice/103/web/2025/02
[28] https://stock.adobe.com/search?k=carbide
[29] https://pubchem.ncbi.nlm.nih.gov/compound/tungsten-carbide
[30] https://www.freepik.com/free-photos-vectors/tungsten-carbide
[31] http://www.tungsten-carbide.com.cn
[32] https://www.istockphoto.com/photos/tungsten-carbide-drill-bits
[33] https://www.britannica.com/science/tungsten-chemical-element
[34] https://www.shutterstock.com/search/tungsten-carbide
[35] https://www.lenntech.com/periodic/elements/w.htm
[36] https://www.hyperionmt.com/en/resources/materies/rationed-carbide/thermal-properties/
[37] https://www.linkedin.com/pulse/properties-tungsten-carbide-shijin-lei-1c
[38] https://www.linde-amt.com/resource-library/articles/tungsten-carbide
[39] https://www.vedantu.com/chemistry/tungsten-carbide
















